ENFERMEDAD DE TRANSMISIÓN SEXUAL: SIFILIS
La sífilis es una enfermedad infecciosa con afectación sistémica causada por el microorganismo Treponema pallidum
subespecie pallidum, perteneciente al Orden Spirochaetales, familia Spirochaetaceae. Son organismos de diámetro exiguo,
con morfología característicamente enrollada. Presentan un movimiento rotatorio y ondulado sobre el eje central de la
bacteria. De los treponemas identificados, solo cuatro causan enfermedad en el ser humano: T. pallidum ssp pallidum (sífilis),
T. pallidum ssp pertenue (frambesia o pian), T. pallidum ssp endemicum (bejel) y Treponema carateum (pinta). Estos cuatro
microorganismos son parásitos obligados del hombre y no se conoce un reservorio animal. Estos treponemas son
morfológica, serológica y químicamente indistinguibles, por lo que las pruebas diagnósticas de la sífilis pueden ser usadas
para diagnosticar la frambesia, el bejel o la pinta. Las enfermedades se diferencian por las manifestaciones clínicas que
producen, le edad de la población afectada, la distribución geográfica y el modo de transmisión. Muchas espiroquetas no
pueden ser cultivadas in vitro, necesitando medios altamente enriquecidos y en un tiempo determinado.
EPIDEMIOLOGÍA
Se producen más de 5 millones de casos nuevos de sífilis en todo el mundo, y la mayoría de las infecciones ocurre en los países de ingresos bajos y medios, donde la infección es endémica y las infecciones congénitas no son infrecuentes.
Los programas de cribado de la OMS han reducido los índices de sífilis materna e infantil en más de un tercio mientras que la sífilis congénita ha sido eliminada en al menos una nación (Cuba).
Por el contrario, en los países de ingresos más elevados, la infección es común y ocurre desproporcionadamente en personas de sectores marginales de la sociedad, como los que viven en la pobreza, con un acceso deficiente a la atención de la salud, o las minorías raciales, étnicas y sexuales.
En los países de altos ingreso, la sífilis se transmite principalmente dentro de estrechas redes sexuales y sociales, una característica que permite observar que aunque la enfermedad es relativamente poco frecuente, más del 15-20% de los casos de sífilis diagnosticados anualmente en EE. UU. fueron diagnosticados antes.
En contraste con la epidemia observada en EE.UU. durante la década de 1990, que en gran medida afectó a personas heterosexuales, en asociación con una epidemia concomitante del consumo de crack cocaína, el resurgimiento actual en Europa occidental y las Américas ha afectado en forma desproporcionada a los hombres que tienen sexo con hombres, y ha estado estrechamente vinculada a la infección por el VIH.
Este perfil de resurgimiento periódico de la sífilis ocurre en períodos de 10 a 15 años y ha sido atribuido a la falta de continuidad de las medidas de control, al cambio en las conductas de riesgo (como el consumo de cocaína crack) y, en a nivel de la población, al crecimiento y disminución de la Inmunidad parcial a la infección del huésped.
Poco después del reconocimiento de la epidemia del VIH, epidemiológicamente, la sífilis ha estado estrechamente asociada a la infección por el VIH. Las úlceras genitales sifilíticas están densamente infiltradas con linfocitos (las principales células objetivo de la infección por el VIH) y así proporcionan una puerta de entrada para la adquisición del VIH y un foco para su transmisión (y la de la sífilis) a otros.
En EE. UU., en 2014, casi el 40% de las personas diagnosticadas con sífilis temprana estaban infectadas con el VIH en el momento del diagnóstico de sífilis y, en algunos lugares, el 3,5-4% de los que eran VIH negativos en el momento de la infección se infectaron con VIH en el año posterior al diagnóstico. La incidencia del VIH en la década posterior al diagnóstico de sífilis el diagnóstico de VIH fue de una incidencia del 20%.
Por otra parte, los investigadores han sugerido que en las personas con VIH, las manifestaciones de sífilis o la respuesta a la terapia recomendada podrían ser diferentes como resultado del efecto del VIH en la inmunidad del huésped. Sin embargo, analizadas más cuidadosamente, las diferencias no suelen ser estadísticamente significativas, reafirmando la variabilidad sustancial de las manifestaciones sifilíticas.
Por otra parte, después de diagnóstico de sífilis, los pacientes que reciben tratamiento para el VIH podrían ser más profundamente estudiados y seguidos con más regularidad, lo que podría introducir un sesgo que favorecería la variabilidad de la presentación de la sífilis y la respuesta a la terapia entre personas confectadas con el VIH.
Aunque la sífilis es una enfermedad infecciosa crónica que puede causar morbilidad a lo largo de su historia natural, la infección es transmisible a otros (con excepción de la infección congénita), solo durante los primeros años de la infección, lo que ha llevado a que las medidas de control se centren en las etapas primaria, secundaria y latente temprana, algunas veces llamada sífilis infecciosa. Después de 2-3 años de infección no tratada, la transmisión es rara y la atención principal se enfoca en la morbilidad individual, incluida la neurosífilis tardía, la sífilis cardiovascular y las infecciones gomatosas.
MANIFESTACIONES CLÍNICAS
Sífilis primaria :El primer signo de la sífilis es una pequeña llaga, que se denomina «chancro». La llaga aparece en el lugar donde la bacteria ingresó al cuerpo. Si bien la mayoría de las personas infectadas por sífilis tienen solo un chancro, algunas personas presentan varios. El chancro suele aparecer alrededor de 3 semanas después de la exposición. Muchas de las personas que tienen sífilis no notan el chancro porque suele ser indoloro y puede estar oculto en la vagina o el recto. El chancro se curará solo en un período de entre 3 y 6 semanas.
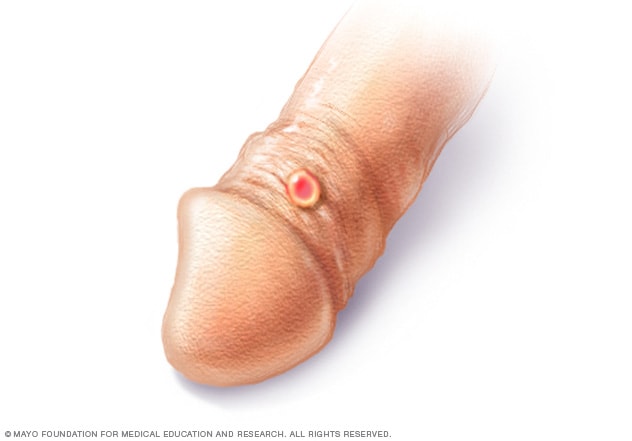
Sífilis secundaria: Luego de unas pocas semanas después de que se cure el chancro, es posible que sientas una erupción cutánea que comienza en el tronco y, finalmente, cubre todo el cuerpo (incluso las palmas de las manos y las plantas de los pies). Esta erupción cutánea no suele producir picazón y puede estar acompañada por llagas que parecen verrugas en la boca y la zona genital. Algunas personas también padecen caída del cabello, dolores musculares, fiebre, dolor de garganta e hinchazón de los ganglios linfáticos. Estos signos y síntomas pueden desaparecer en pocas semanas o pueden aparecer y desaparecer de forma repetida durante hasta un año.
Sífilis latente : Si no recibes tratamiento para la sífilis, la enfermedad pasa de la etapa secundaria a la etapa latente (oculta), en la cual no tienes síntomas. La etapa latente puede durar años. Es posible que los signos y síntomas no vuelvan a presentarse nunca, o bien la enfermedad puede progresar a la tercera etapa (etapa terciaria).
Sífilis terciaria (tardía) :Entre el 15 y el 30 por ciento de las personas infectadas por sífilis que no reciben tratamiento presentarán complicaciones conocidas como sífilis terciaria (tardía). En la etapa tardía, la enfermedad puede dañar el cerebro, nervios, ojos, corazón, vasos sanguíneos, hígados, huesos y articulaciones. Estos problemas pueden ocurrir muchos años después de la infección original que no se trató.
Sífilis congénita : Los bebés de las mujeres con sífilis pueden infectarse mediante la placenta o durante el parto. La mayoría de los recién nacidos con sífilis congénita no presentan síntomas, aunque en algunos casos se puede presentar una erupción cutánea en las palmas de las manos y las plantas de los pies. Los síntomas posteriores pueden comprender sordera, deformidades en los dientes y la nariz en silla de montar (cuando colapsa el puente nasal).

Neurosífilis: En términos generales, la neurosífilis es una superposición de alteraciones meningovasculares parenquimatosas. El
diagnóstico de la neurosífilis asintomática se realiza en pacientes que no tienen manifestaciones clínicas pero sí
anormalidades del líquido cefalorraquídeo (LCR), como pleocitosis, aumento de las proteínas, disminución de la glucosa o una
respuesta positiva en la prueba VDRL, con lo cual se hace necesario la punción lumbar para poder establecerlo. La
neurosífilis meningovascular se debe al desarrollo de una endoarteritis obliterante que afecta a los vasos sanguíneos de las
meninges, cerebro, cordones espinales, etc., que provocará múltiples infartos. La parenquimatosa se debe a la destrucción de
las células nerviosas, sobre todo de la corteza cerebral.
Las manifestaciones clínicas consisten en paresia, afasia, manifestaciones psiquiátricas, etc. Destacan la tabes dorsal y el
signo de la pupila de Argyll-Robertson. En la tabes dorsal, el daño se produce principalmente por una desmielinización de la
columna posterior, ganglios y raíces dorsales que provocará la aparición de un cuadro clínico de ataxia, parestesias,
incontinencia fecal, impotencia, etc. Las alteraciones oculares son frecuentes, destacando el signo antes mencionado, que
consiste en una pupila pequeña e irregular que acomoda para la visión de cerca, pero no ante estímulos luminosos. En un
período de meses a años puede aparecer una atrofia óptica. Cualquier par craneal puede estar afectado, destacando el VII y
el VIII. Oído y ojo pueden estarlo afectos en cualquier estadio de la enfermedad, incluso en la sífilis congénita.
DIAGNÓSTICO DE LABORATORIO
Detección directa de T. pallidum
Examen en fresco con microscopía de campo oscuro. Es el método de diagnóstico más rápido y directo en las fases primaria,
secundaria y congénita precoz. La muestra ideal es el exudado de las lesiones, como el chancro, condiloma plano y lesiones
mucosas, ya que contienen gran cantidad de treponemas; también pueden observarse a partir del material aspirado de los
ganglios linfáticos. La muestra debe ser lavada con suero salino sin aditivos bactericidas. El treponema aparecerá
moviéndose en espiral con una ondulación característica sobre su punto medio. Es importante señalar que, en las lesiones
bucales o anales es difícil diferenciar T. pallidum de otros treponemas no patógenos, por lo que la técnica de campo oscuro no
es aplicable. Para excluir el diagnóstico se requieren tres exámenes negativos.
Inmunofluorescencia directa (DFA-TP). Consiste en la tinción con anticuerpos monoclonales o policlonales fluorescentes
dirigidos frente a T. pallidum en los frotis desecados de lesiones sospechosas, una vez fijados con acetona o metanol. Esta
técnica es obligada para el examen de las lesiones orales, por las razones antes señaladas.
Demostración en tejidos. Requiere materiales obtenidos por biopsia, sobre los que se lleva a cabo una impregnación
argéntica, o bien una tinción inmunofluorescente (DFAT-TP) o inmunoenzimática específica. La DFAT-TP utiliza un anticuerpo
monoclonal muy específico de T. pallidum. Se suele utilizar para muestras cutáneas de sífilis secundaria o estadios sifilíticos
tardíos (goma), así como en los tejidos afectados de cerebro, placenta, cordón umbilical o piel en la sífilis congénita.
Cultivo de T. pallidum. El único método útil para aislar T. pallidum es la prueba de inoculación en el conejo (RIT). Esta técnica
se considera como de referencia para el resto de las pruebas diagnósticas de la sífilis. Por su dificultad y peligrosidad sólo se
realiza en laboratorios de referencia muy específicos y de investigación.
Técnicas de biología molecular. Los métodos de amplificación de ácidos nucleicos aumentan la sensibilidad de los métodos
de detección de T. pallidum, siendo útiles en los casos en que el resto de pruebas muestran una baja sensibilidad, como es el
caso del diagnóstico de la sífilis congénita, neurosífilis, en la sífilis primaria temprana y cuando existe la necesidad de
distinguir entre una reinfección y una infección antigua.
Detección indirecta de T. pallidum:
pruebas serológicas
Se detectan dos tipos de anticuerpos: los llamados reagínicos, no específicos o no treponémicos, y los treponémicos o
específicos (IgG e IgM).
Pruebas reagínicas o no treponémicas. Los anticuerpos reagínicos son de tipo IgG e IgM dirigidos frente a un antígeno
lipoideo que es el resultado de la interacción de T. pallidum con los tejidos del huésped (cardiolipina-colesterol-lecitina).
Aunque los resultados falsos positivos son bastante frecuentes, son los mejores métodos de diagnóstico serológico en la sífilis
latente temprana y en la tardía. Las pruebas reagínicas se dividen en:
● Floculación microscópica: VDRL (Venereal Disease Research Laboratory), USR.
● Floculación macroscópica: RPR prueba en tarjeta de reaginas plasmáticas rápidas, ART, TRUST, RST.
● Enzimoinmunoensayo (ELISA) no trepónemico: utiliza como antígeno el del VDRL.
El VDRL es una prueba no treponémica normalizada en la cual el suero, previamente inactivado a 56 ºC, se enfrenta en un
portaobjetos con un antígeno de cardiolipina-colesterol-lecitina para observar su capacidad de floculación. Tanto el RPR como
el VDRL son buenos marcadores de la infección en su fase aguda y útiles en el control de la respuesta al tratamiento en el
paciente con inmunidad intacta, aunque son poco específicos. El RPR ha pasado a ser la prueba de cribado habitual para la
selección de sueros en los laboratorios y en los bancos de sangre, puesto que se trata de una técnica más sencilla, requiere
menor cantidad de suero y no hace falta calentarlo. El VDRL es la prueba de elección para el diagnóstico de la neurosífilis en
muestras de LCR. La mayor utilidad del ELISA es el cribado de poblaciones, por la gran cantidad de muestras que puede
procesar al mismo tiempo. Como contrapartida negativa, no permite obtener resultados cuantitativos.
TRATAMIENTO
La eficacia del tratamiento es bien conocida. Sin embargo, para que sea adecuado hay que tener en cuenta una serie de
recomendaciones obtenidas de las infecciones experimentales: a) que T. pallidum se regenerará al cabo de 18-24 h si los
niveles de penicilina en sangre están por debajo de la concentración mínima inhibitoria
b) que se necesita una concentración
de penicilina >0.03 µg/ml de penicilina para asegurar un efecto bactericida
y c) que para curar una sífilis precoz se requiere
una concentración adecuada mantenida durante 7 días. Durante muchos años se ha tenido a la penicilina benzatina como el
tratamiento de elección, excepto en el caso de una invasión del LCR (se han aislado treponemas en LCR de pacientes con
chancro primario, lo que refleja la espiroquetorraquia). Por lo tanto, el tratamiento actual de la sífilis con una combinación
antibiótica o un régimen prolongado asegura que esta secuela, la más importante de la sífilis, no ocurrirá. Esto es
especialmente importante en los pacientes inmunodeprimidos.
Sífilis temprana (primaria, secundaria)
● Penicilina G benzatina 2.400.000 UI intramuscular por semana en 3 dosis.
● Doxiciclina, 100 mg oral, 21 d.
● Otros: amoxicilina + probenecid, ceftriaxona, penicilina G procaína + probenecid.
● En los alérgicos a la penicilina: doxiciclina o eritromicina.
Sífilis tardía y neurosífilis
● Penicilina G sódica .
● Otros: amoxicilina + probenecid, doxiciclina, ceftriaxona y penicilina G procaína + probenecid.
En los alérgicos a la penicilina se recomienda la desensibilización y el tratamiento con penicilina y, como alternativa,
el cloranfenicol.
Sífilis en el embarazo: Las gestantes deberían recibir tratamiento adecuado al estadio de la sífilis. Es de elección la penicilina, incluso en los
alérgicos, donde es necesaria la desensibilización, porque tanto las tetraciclinas como el cloranfenicol no se recomiendan
explícitamente.
Sífilis congénita
Se recomienda efectuar el tratamiento en aquellos niños nacidos de madres no tratadas correctamente, y es de elección la
penicilina G sódica o la penicilina G procaína.
Sífilis en los inmunodeprimidos: Estos pacientes deben ser tratados siguiendo el mismo esquema que para la neurosífilis.
Infección persistente
Hay pacientes en los que, a pesar de un tratamiento adecuado, las pruebas reagínicas no llegan a negativizarse. Al parecer,
se debe a que en estos pacientes quedan treponemas en lugares en los que se alcanzan con dificultad niveles adecuados de
antibiótico: cámara anterior del ojo, LCR, laberinto, etc.
Seguimiento del tratamiento: En todos los pacientes con sífilis precoz y congénita hay que repetir las pruebas no treponémicas cuantitativas (RPR o VDRL)
al cabo de uno, tres, seis y 12 meses del tratamiento de la sífilis. En los pacientes infectados por el VIH, además de estos
controles, se efectuarán otros adicionales en el segundo y noveno mes después del tratamiento